10 Reaksi Kimia yang Menakjubkan
Kimia adalah subjek yang sangat menarik. Cara atom-atom berperilaku menentukan segala sesuatu dari makanan yang kita makan dan pakaian yang kita kenakan, hingga pembentukan genetik kita dan bagaimana kita merasa. Kesederhanaan dari tabel periodik menjelaskan hanya 118 unsur yang membentuk setiap materi yang dikenal. Unsur-unsur ini bereaksi dalam berbagai cara, membentuk ratusan juta senyawa, dua atau lebih unsur terikat bersama, dan memberikan kita keragaman bahan yang membentuk dunia kita. Beberapa reaksi merupakan reaksi fisik, bukan reaksi kimia, dan cara untuk mengetahui bahwa itu reaksi kimia yaitu apakah atau tidak terjadi perubahan dalam rumus kimia.
Pencairan es adalah perubahan fisik karena air adalah zat yang sama seperti es, hanya dalam keadaan wujud yang berbeda dari materi. Pembakaran batu bara, di sisi lain, adalah perubahan kimia, batu bara dan oksigen terbakar dan menghasilkan karbon monoksida. Reaksi kimia mendorong perubahan satu substansi ke substansi lain dan reaksi kimia umumnya diidentifikasi dengan adanya perubahan warna atau pelepasan energi yang sering dalam bentuk panas, ledakan, cahaya dan suara. Tidak mungkin membahas semua reaksi kimia yang terjadi di alam semesta kita dalam satu artikel, jadi kami telah memilih sepuluh reaksi yang menonjol dan memiliki hasil yang dramatis.
1. Peleleh Logam - Reaksi Termit
Bahan: Aluminium (Al); Besi Oksida (Fe2O3)
Inti Proses: Penggantian Tunggal
 |
| The Metal Melter |
Termit merupakan reaksi panas yang terdiri dari bubuk logam dan oksida logam (paling sering aluminium dan besi oksida); yang terakhir lebih dikenal sebagai karat. Karakteristik reaksi termit yaitu tidak begitu banyak ledakan, sebaliknya memiliki kemampuan untuk memanaskan area yang sangat kecil hingga suhu yang sangat tinggi. Anda mungkin tidak terpikir bahwa logam sebagai pembakar yang sangat mudah, tetapi dalam kondisi yang tepat dan suhu pengapian yang sangat tinggi, itu dapat terjadi.
Reaksi termit digunakan untuk pengelasan rel kereta bersama-sama dan suhu setinggi 2.500 derajat Celsius (4.532 derajat Fahrenheit) dapat dicapai. Karena panas tinggi, produk reaksi termit berbentuk cair, membuatnya sempurna untuk pengelasan. Reaksi termit memiliki pasokan oksigen sendiri dari oksida logam, sehingga dapat bekerja bahkan tanpa adanya udara, seperti di air dan di ruang angkasa.
Aluminium dan besi oksida yang dipanaskan, sering dengan pita magnesium sebagai pengaman, dan oksigen dari besi oksida memecah ikatan untuk bergabung dengan aluminium sehingga membentuk aluminium oksida dan besi. Topeng khusus dengan pelindung UV harus dipakai saat pengelasan karena intensitas radiasi yang tinggi.
2. Pengkristal – Kristal Tembaga Sulfat
Bahan: Tembaga Sulfat Pentahidrat (CuSO4 * 5H2O); Air (H2O)
* (Berhati-hati karena tembaga sulfat dapat mengakibatkan iritasi ringan)
 |
| The Crystalliser |
Apa yang kurang dalam daya ledak, tembaga sulfat dapat membuat lebih daripada penampilannya, menghasilkan kristal biru cerah ketika bentuk terhidrasinya dilarutkan dalam air panas. Tembaga sulfat adalah jenis dari garam, dan yang paling sering ditemui sebagai bubuk yakni tembaga sulfat pentahidrat (CuSO4* 5H2O). Ini adalah cara untuk mengekspresikan lima molekul air yang melekat pada molekul tembaga sulfat, itu terhidrasi.
Untuk pembentukan kristal biru, tembaga sulfat pentahidrat ditambahkan ke air panas sampai titik di mana tidak ada lagi yang bisa larut. Hal ini disebut sebagai larutan jenuh, dan larutan yang lebih panas dapat melarutkan lebih banyak tembaga sulfat daripada yang dingin. Ketika larutan mulai dingin, beberapa tembaga sulfat tidak dapat lama lagi dalam keadaan terlarut, sehingga molekul berkumpul dalam pola berulang yang terorganisir, membentuk kristal.
Hal tersebut adalah contoh dari perubahan fisik karena bahan ini mengubah struktur dan bukan susunannya. Menangguhkan kawat nilon ke dalam larutan membuat permukaan kristal untuk terkait padanya, mendorong pertumbuhan. Akhirnya air menguap, tetapi tembaga sulfat tidak bisa jadi tembaga sulfat dipaksa ke dalam ruang yang bahkan lebih kecil. Molekul-molekul tembaga sulfat terus mengkristal sampai tidak ada air yang tersisa.
3. Penyala Api – Pembakaran Hidrogen
Bahan: Hidrogen (H2); Oksigen (O2)
Inti Proses: Redox
 |
| The FireStarter |
Hidrogen (H2) merupakan unsur yang paling ringan, unsur yang paling melimpah di alam semesta, namun itu juga merupakan salah satu yang paling mudah terbakar. Hidrogen cepat untuk terbakar dengan adanya oksigen (O2) dan bisa sangat eksplosif. Digunakan sebagai bahan bakar utama untuk pembakaran ketika meluncurkan pesawat ulang-alik, pembakaran yang dihasilkan sangatlah kuat.
Ketika hidrogen terbakar, sejumlah besar panas dan cahaya yang dilepaskan. Cahaya yang dipancarkan dari hidrogen murni dan reaksi oksigen terutama ultraviolet, membuat api hampir tak terlihat. Namun dalam kenyataannya, sering terdapat bahan lain yang ditambahkan, membuat api terlihat. Air adalah produk limbah dari pembakaran hidrogen, karena oksigen dan hidrogen adalah dua bahan dalam air. Pembakaran hidrogen cair dan oksigen digunakan untuk meluncurkan roket, oleh karena itu adalah uap air, bukan asap, yang anda lihat keluar dari knalpot selama lepas landas.
Para ilmuwan sekarang bekerja menggunakan pembakaran hidrogen sebagai tenaga mobil dan mesin lainnya. Kesulitannya adalah memerlukan sejumlah besar energi awal untuk memperoleh reaksi yang terjadi. Hal ini membutuhkan jauh lebih banyak energi untuk memulainya, katakanlah, bahan bakar fosil tradisional. Hidrogen jarang ditemukan di Bumi dalam bentuk murni, karena lebih memilih untuk bergabung dengan unsur-unsur lain dan tentu saja banyak terdapat pada air.
4. Umpan Bom - Magnesium dan Teflon
Bahan: Magnesium (Mg); Teflon ([C2F4] n)
Inti Proses: Redox
Magnesium (Mg) merupakan elemen yang sangat reaktif yang terbakar di 3.100 derajat Celsius (5.612 derajat Fahrenheit), mengeluarkan cahaya putih yang kuat. Selain cahaya yang tampak, magnesium memancarkan inframerah (IR) ketika terbakar, sehingga cocok untuk digunakan dalam militer seperti umpan flare (suar). Seperti semua hal, magnesium harus dihadapkan dengan sebuah pengoksidasi ketika dibakar, yaitu bahan yang mengambil elektron dari bahan bakar yang memungkinkan reaksi terjadi.
Flare terbuat dari Teflon ([C2F4] n) dan magnesium, dan fluor dalam Teflon yang mengoksidasi magnesium. Fluor adalah pengoksidasi yang lebih kuat daripada oksigen, karena ingin menerima elektron lebih daripada oksigen, memungkinkan suhu yang lebih tinggi dari pembakaran. Rudal pencari panas mengunci ke cahaya inframerah yang dipancarkan oleh mesin dalam pesawat, namun umpan flare magnesium membuang cahaya IR jauh lebih banyak daripada mesin pesawat, ini cukup efektif untuk membingungkan sistem bimbingan pencari panas dari rudal dan berharap menghalangi senjata dari target.
 |
| The Bomb Decoy |
Magnesium (Mg) merupakan elemen yang sangat reaktif yang terbakar di 3.100 derajat Celsius (5.612 derajat Fahrenheit), mengeluarkan cahaya putih yang kuat. Selain cahaya yang tampak, magnesium memancarkan inframerah (IR) ketika terbakar, sehingga cocok untuk digunakan dalam militer seperti umpan flare (suar). Seperti semua hal, magnesium harus dihadapkan dengan sebuah pengoksidasi ketika dibakar, yaitu bahan yang mengambil elektron dari bahan bakar yang memungkinkan reaksi terjadi.
Flare terbuat dari Teflon ([C2F4] n) dan magnesium, dan fluor dalam Teflon yang mengoksidasi magnesium. Fluor adalah pengoksidasi yang lebih kuat daripada oksigen, karena ingin menerima elektron lebih daripada oksigen, memungkinkan suhu yang lebih tinggi dari pembakaran. Rudal pencari panas mengunci ke cahaya inframerah yang dipancarkan oleh mesin dalam pesawat, namun umpan flare magnesium membuang cahaya IR jauh lebih banyak daripada mesin pesawat, ini cukup efektif untuk membingungkan sistem bimbingan pencari panas dari rudal dan berharap menghalangi senjata dari target.
Api magnesium tidak dapat dipadamkan dengan air, karena magnesium bereaksi dengan air untuk menghasilkan gas hidrogen, yang ada hanyalah akan mengintensifkan api. Malah, pasir kering yang umumnya digunakan untuk menghentikan reaksi. Kegunaan lain dari magnesium yaitu sebagai sumber penerangan di fotografi flash dan kembang api.
5. Pemadat – Sodium Asetat Supersaturasi
Bahan: Sodium/Natrium Asetat (NaC2H3O2); Air (H2O)
Inti Proses: Kristalisasi
Sodium asetat (NaC2H3O) dipanaskan dalam air kemudian didinginkan memiliki sifat kristalisasi yang tidak biasa ke dalam bentuk padat ketika terganggu/terguncang. Hal ini dapat dituangkan dari gelas dalam bentuk cairan dan setelah menyentuh permukaan menjadi bentuk padat yang panas bila disentuh, maka sering disebut juga dengan es panas. Sodium asetat adalah garam yang larut dalam air. Pemanasan sekitar 100 derajat Celsius (212 derajat Fahrenheit) kemudian pendinginan campuran dari keduanya memungkinkan lebih banyak sodium asetat untuk larut dan membentuk larutan jenuh. Larutan yang ada dalam keadaan metastabil, dianalogikan dengan bola yang bertengger di puncak bukit, di mana dorongan sedikit akan membuatnya menggelinding ke bawah.
 |
| The Solidifier |
Sodium asetat (NaC2H3O) dipanaskan dalam air kemudian didinginkan memiliki sifat kristalisasi yang tidak biasa ke dalam bentuk padat ketika terganggu/terguncang. Hal ini dapat dituangkan dari gelas dalam bentuk cairan dan setelah menyentuh permukaan menjadi bentuk padat yang panas bila disentuh, maka sering disebut juga dengan es panas. Sodium asetat adalah garam yang larut dalam air. Pemanasan sekitar 100 derajat Celsius (212 derajat Fahrenheit) kemudian pendinginan campuran dari keduanya memungkinkan lebih banyak sodium asetat untuk larut dan membentuk larutan jenuh. Larutan yang ada dalam keadaan metastabil, dianalogikan dengan bola yang bertengger di puncak bukit, di mana dorongan sedikit akan membuatnya menggelinding ke bawah.
Pemicunya bisa dengan menuangkan cairan keluar dari wadah, atau menambahkan benih kristal, menyebabkan sodium asetat yang terlarut untuk keluar dari larutan dan kembali ke bentuk padat. Dalam analogi kami ini seperti bola menggelinding menuruni bukit hingga mencapai di tanah datar dan keadaan energi yang lebih rendah.
Sepanjang jalan, sodium asetat padat menyerap tiga molekul air, menjadi sodium asetat trihidrat (NaC2H3O2* 3H2O). Molekul air ini tidak secara kimia terikat pada sodium asetat, yang menunjukkan perubahan fisik. Proses ini adalah eksotermik (yakni melepaskan panas) dan sebagai hasilnya, itu sering digunakan pada penghangat tangan.
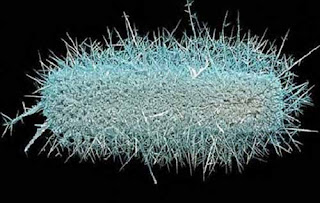
6. Pembuat Fraktal – Tembaga dan Perak Nitrat
Bahan: Silver/Perak Nitrat (AgNO3); Tembaga (Cu); Air (H2O)
Mencampur perak nitrat dan tembaga adalah salah satu eksperimen kimia yang paling terkenal, dengan membintangi banyak ilmu pelajaran sekolah di seluruh dunia. Percobaan ini meliputi mempertemukan tembaga (biasanya kawat tembaga) ke perak nitrat/larutan air dan menunggunya di sana selama beberapa jam.
Kombinasi dari keduanya memicu reaksi penggantian tunggal, di mana tembaga berubah dari bentuk unsur (Cu) ke bentuk ion biru berair (Cu + [aq]), sedangkan ion perak (Ag + [aq]) dalam larutan perak nitrat akan berubah ke dalam bentuk unsur logam mereka (Ag) dan diendapkan ke kawat. Endapan perak ini terus tumbuh dari tembaga dalam serangkaian kristal (yang berbentuk seperti fractal) hingga semua tembaga yang dapat bereaksi dalam larutan habis, meninggalkan produk akhir berupa perak dan tembaga nitrat.
Alasan reaksi penggantian ini terjadi adalah bahwa atom dalam tembaga teroksidasi ketika dipertemukan ke dalam larutan perak nitrat, kehilangan elektron dan membentuk ion tembaga, sedangkan ion perak dalam larutan nitrat dikurangi (yaitu mereka mendapatkan elektron) menjadi unsur perak. Hal yang menarik adalah bahwa setelah kristal perak telah tumbuh, dapat dipisah dari tembaga, dikeringkan dan kemudian ditampilkan sebagai bagian dari seni fraktal.
7. Ramuan Penyihir - Potasium dan Air
Bahan: Potasium/Kalium (K); Air (H2O)
Inti Proses: Redox
Memasukkan gumpalan kalium ke dalam cawan air maka akan mengeluarkan cahaya merah muda, sangat panas dan melintas di permukaan dengan cepat. Percobaan favorit di banyak kelas sains, kalium adalah logam yang sangat reaktif yang bereaksi keras dengan adanya oksigen dan air. Membentuk kalium hidroksida (KOH) dan gas hidrogen (H2).
 |
| The Witch's Potion |
Memasukkan gumpalan kalium ke dalam cawan air maka akan mengeluarkan cahaya merah muda, sangat panas dan melintas di permukaan dengan cepat. Percobaan favorit di banyak kelas sains, kalium adalah logam yang sangat reaktif yang bereaksi keras dengan adanya oksigen dan air. Membentuk kalium hidroksida (KOH) dan gas hidrogen (H2).
Atom kalium memiliki 19 elektron, salah satu yang sendiri berada di kulit terluar. Hal ini membuat kalium sangat tertarik untuk kehilangan elektron sehingga akan memiliki kulit luar yang lengkap dan lebih stabil. Ketika reaksi dimulai, panas yang keluar cukup untuk menyalakan gas hidrogen, yang kemudian bereaksi dengan oksigen untuk menghasilkan air. Kalium sangat reaktif yang harus disimpan dalam kerosin (minyak tanah), agar tidak bersentuhan dengan uap air di udara. Bahkan oksigen di udara cukup untuk menyebabkan kalium secara spontan terbakar. Karena kalium sangat reaktif, kalium tidak ditemukan dalam bentuk unsur, tetapi umumnya sebagai senyawa.
8. Jeritan Jeli Bayi – Kalium Klorat dan Jeli Bayi
Bahan: Kalium Klorat (KCLO3); Jeli Bayi (Sirup Glukosa, Gula, Air, Gelatine, dan Perasa)
Melihat jeli bayi bertemu kehancurannya di tangan potasium klorat adalah urusan yang spektakuler. Ada kelimpahan energi dalam jeli bayi yang disimpan sebagai gula, melepaskan api yang kuat dan jeritan yang tajam ketika kalium klorat ditambahkan ke dalam campuran.
Potasium klorat merupakan pengoksidasi kuat, berbentuk seperti bubuk putih dan biasanya digunakan dalam kembang api dan bahan peledak. Bagian dari klorat menggambarkan atom oksigen terikat pada atom klorin, dan rumus kimia KCLO3. Klorat berbasis oksida merupakan oksida yang lebih efisien dibandingkan pada mesiu dan potasium klorat, perlu ditangani sangat hati-hati karena kemampuannya yang tak terduga untuk spontan terbakar.
Reaksi terjadi ketika sejumlah kecil potasium klorat ditempatkan dalam tabung reaksi dan dipanaskan sampai menjadi cairan bening. Tak perlu dikatakan, layar keamanan dan kacamata adalah suatu keharusan. Jeli bayi ditempatkan dengan penjepit ke dalam tabung dan langsung menghasilkan api hidup, mengeluarkan teriakan secara intens dan banyak asap. Reaksi dapat berlangsung hingga 20 detik dan mengeluarkan asap berbahaya sehingga ventilasi juga diperlukan.
9. Gonggongan Anjing – Karbon disulfida dan Nitrous Oksida
Bahan: Karbon disulfida (CS2); Oksida nitrat (N2O)
Reaksi gonggongan anjing merupakan akibat dari memicu karbon disulfida (CS2) dicampur dengan oksida nitrat (N2O) - yang terakhir ini juga lebih dikenal sebagai gas tertawa. Reaksi ini menghasilkan kilatan cahaya terang ungu-kebiruan dan panas, dan, yang lebih aneh, suaranya seperti anjing menggonggong.
Gas oksida nitrat adalah sumber oksigen (yaitu pengoksidasi) yang dibutuhkan untuk membakar bahan bakar cair tidak berwarna, karbon disulfida. Ketika reaksi berlangsung di ruang tertutup (seperti tabung panjang) sebagian energi akan diubah untuk membentuk riam tapi dengan suara gonggongan yang keras, karena fluktuasi tekanan. Ini adalah contoh dari reaksi yang membuat unsur-unsur dari senyawa: dalam hal ini lapisan kuning belerang dan gas nitrogen adalah unsur-unsur yang tersisa di belakangnya.
Karbon disulfida ditemukan di alam sebagai produk dari proses metabolisme pada tanaman, dan juga letusan gunung berapi. Oksida nitrat juga dibentuk secara alami dari beberapa spesies bakteri, ditambah melalui industri dan pertanian, dan ini menguras ozon di stratosfer. Digunakan di masa lalu sebagai metode fotografi flash, flash (kilat) yang dihasilkan begitu cerah yang membuat banyak orang ketika di foto akan sering terkejut. Bau menyengat yang mungkin dihasilkan senyawa sulfur tidak membuat ini popular dengan baik.
10. Roket Manis – Kalium Nitrat dan Gula
Bahan: Kalium Nitrat (KNO3); Sukrosa (C12H22O11)
Inti Proses: Redox
Ada sesuatu keanehan yang memuaskan saat menyaksikan tampilan asap yang mudah menguap, warna dan api dilepaskan oleh campuran potasium nitrat, gula dan panas. Jumlah api bervariasi, tetapi selalu ada banyak asap. Anda kemungkinan besar melihat reaksi ini saat pertunjukkan kembang api, atau dari asap yang disebarkan pesawat akrobat di mana zat pewarna sering ditambahkan sebagai efek.
Kalium nitrat (KNO3), alias saltpetre adalah hal penting dalam setiap komposisi kembang api, itu salah satu bahan utama dalam bubuk mesiu. Kalium nitrat bekerja sebagai pengoksidasi, melepaskan oksigen dan memicu pembakaran bahan bakar.
Seperti yang terlihat di jeritan jeli bayi, gula merupakan bahan bakar yang sangat efektif; mengandung energi yang 'terbakar' dalam tubuh kita dan diubah ke energi yang berguna bagi kita untuk melakukan aktivitas fisik. Ketika panas diberikan pada saltpetre dan gula, salpetre kehilangan atom oksigen, bertransisi dari KNO3 menjadi KNO2 dan mengoksidasi gula. Gula terbakar, melepaskan asap yang cepat mengembang dan dapat menghasilkan daya dorong yang cukup untuk mengangkat roket kecil.
Diperbarui pada 22 Januari 2017.










Tidak ada komentar:
Posting Komentar
Silahkan berkomentar dengan baik dan bijak, menghormati satu sama lain. Terima kasih.